Das Enzym mit dem eisernen Herzen
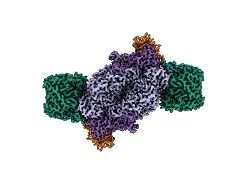
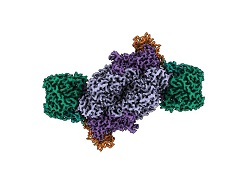
Nitrogenasen sind die einzigen biologischen Katalysatoren (Enzyme), die in
der Lage sind, Stickstoff aus der Luft in bioverfügbaren Stickstoff
umzuwandeln - ein Prozess, der für alles Leben auf der Erde unerlässlich
ist. Nun ist es Forschenden des Max-Planck-Instituts für terrestrische
Mikrobiologie in Marburg mit Hilfe der Kryo-Elektronenmikroskopie
gelungen, die Struktur des Eisen-Nitrogenase-Komplexes in seiner
Gesamtheit aufzuklären und seine einzigartige molekulare Architektur zu
enthüllen. Die Ergebnisse bilden eine wichtige Grundlage für das
Verständnis der Struktur-Funktionsbeziehungen des Enzyms und zukünftige
Entwicklungen neuer Biokatalysatoren für nachhaltige Biotechnologie.
Stickstoff ist Bestandteil vieler wichtiger Biomoleküle, wie der DNA, aber
auch der Aminosäuren, aus denen Proteine aufgebaut sind. Bevor Stickstoff
in Biomoleküle eingebaut werden kann, muss er zunächst bioverfügbar
gemacht werden. In der Natur ist nur eine einzige Klasse von Enzymen,
sogenannte Nitrogenasen, in der Lage, diese wichtige Umwandlung
durchzuführen.
Nitrogenasen können auch CO2 umwandeln
Kürzlich wurde gezeigt, dass Nitrogenasen auch Kohlendioxid (CO2) und
Kohlenmonoxid zu Kohlenwasserstoffen wie Methan oder Ethylen reduzieren
können, was prinzipiell die Möglichkeit eröffnet, Kohlenstoffabfälle in
Kohlenwasserstoffprodukte umzuwandeln. Innerhalb der Familie der
Nitrogenasen ist die Eisen(Fe)-Nitrogenase das Isoenzym mit der höchsten
natürlichen Fähigkeit zur CO2-Reduktion. Die molekulare Architektur, die
diese Reaktionen ermöglicht, war bislang jedoch unbekannt - ein Problem,
das die Arbeitsgruppe von Dr. Johannes Rebelein am Max-Planck-Institut für
terrestrische Mikrobiologie lösen wollte.
Die Forschenden nutzten eine gentechnisch veränderte Variante des
Purpurbakteriums Rhodobacter capsulatus als Modellorganismus, um die Fe-
Nitrogenase zu reinigen und biochemisch zu charakterisieren. Durch die
Kombination von anaerober Biochemie und kryogener Elektronenmikroskopie in
Zusammenarbeit mit der Central Electron Microscopy Facility am Max-Planck-
Institut für Biophysik in Frankfurt gelang es ihnen, die Struktur des
gesamten Enzymkomplexes aufzuklären.
Die Ergebnisse zeigen, dass der Cofaktor im aktiven Zentrum - im Gegensatz
zu anderen Nitrogenase-Typen - kein anderes Metall als Eisen enthält.
Außerdem weist die Architektur der Fe-Nitrogenase besondere strukturelle
Merkmale auf, die für die einzigartigen katalytischen Eigenschaften der
Fe-Nitrogenase verantwortlich sein könnten.
Unterschiede jenseits des aktiven Zentrums
"Wir hatten erwartet, dass der Hauptunterschied zwischen der Fe-
Nitrogenase und anderen Nitrogenase-Formen, wie der Molybdän-Nitrogenase,
in der Architektur des Cofaktors im aktiven Zentrum und seiner
unmittelbaren Umgebung liegt. Zu unserer Überraschung stellten wir jedoch
fest, dass die aktiven Zentren der drei Nitrogenase-Isoformen, trotz ihrer
Unterschiede in den katalytischen Eigenschaften, einander sehr ähnlich
sind", sagt Frederik Schmidt, Doktorand im Labor von Johannes Rebelein und
Erstautor der Studie. Wenn es aber keine auffälligen Unterschiede im
Bereich des aktiven Zentrums gibt, welche Merkmale könnten dann die
einzigartige Reaktivität dieses Enzyms erklären?
Die Autorinnen und Autoren weisen auf zwei strukturelle Besonderheiten
hin: Zum einen besitzt das Enzym eine zusätzliche Untereinheit, die so
genannte G-Untereinheit. Diese Untereinheit war zwar schon früher
beschrieben worden, ihre Funktion blieb jedoch rätselhaft. Basierend auf
ihrer neuen Struktur schlagen die Forschenden drei mögliche Funktionen für
die G-Untereinheit vor, nämlich die Koordination des Elektronentransfers,
die Kanalisierung des Substrats und die Stabilisierung des Cofaktors im
aktiven Zentrum.
Veränderte Symmetrie könnte Grund für höhere Reaktivität sein
Nitrogenasen sind Enzyme, deren Funktion durch die Interaktion zweier
symmetrischer Hälften zustande kommt. Als die Forschenden jedoch die
Struktur der Fe-Nitrogenase mit der bereits gelösten Struktur der Mo-
Nitrogenase überlagerten, stellten sie fest, dass bei letzterer die
Symmetrie verändert ist. "Man nimmt an, dass die beiden symmetrischen
Hälften miteinander kommunizieren, um den katalytischen Mechanismus des
Enzyms zu koordinieren. Die veränderte Symmetrie, die wir in der Fe-
Nitrogenase beobachtet haben, könnte ihre besondere Reaktivität erklären,“
erklärt Luca Schulz, Mit-Erstautor der Studie.
Wie genau diese strukturellen Unterschiede den katalytischen Mechanismus
der Fe-Nitrogenase beeinflussen, wird eine der Schlüsselfragen für die
Zukunft sein. Die Forscher hoffen, den molekularen Mechanismus des Enzyms
weiter aufklären zu können, was zur Entwicklung neuartiger
Biokatalysatoren für die nachhaltige Stickstoffassimilation und
CO2-Umwandlung beitragen könnte.





